Shimadzu于4月20日推出用于医疗机构的新型冠状病毒检测试剂盒
Shimadzu新闻稿
Shimadzu将发布“新型冠状病毒检测试剂盒”,该试剂盒已于4月20日开发了一段时间。目前,它仅在日本销售,但我们将进行准备工作,以期在5月以后向海外出口。 当前,通过基因扩增法(PCR法)检测新的冠状病毒(SARS-CoV-2)时,需要从诸如鼻咽拭子的样品(样品)中提取和纯化RNA的复杂工作。是必需的。这阻碍了对大量样品的快速检查。通过使用该试剂盒,可以省去RNA提取和纯化步骤,从而可以显着减少测试所需的工作量,并且整个PCR测试过程(耗时2小时以上)可以减少到大约1小时,是传统PCR测试的一半。 。即使使用96样品PCR装置测试了96个样品,也可以在不到一个半小时的时间内完成。另外,由于不需要手动操作,因此也有助于防止人为错误。 “新冠状病毒检测试剂盒”是根据我们最初的Ampdirect技术* 1开发的,并与美国国家传染病研究所手册* 2保持一致。该技术指出:“由于可以抑制生物样品中包含的蛋白质和多糖等PCR抑制剂的作用,因此可以将生物样品直接添加到PCR反应溶液中,而无需提取和纯化DNA和RNA。”是的。 Shimadzu开发并销售了使用Ampdirect技术检测病原菌的试剂,例如肠出血性大肠杆菌,沙门氏菌,志贺氏菌和诺如病毒。我们开发了一种病毒检测试剂。
新产品功能
1。 快速简便的可操作性
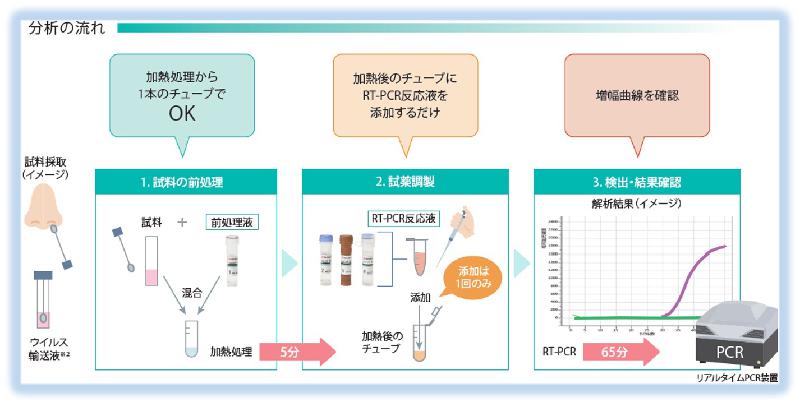
该试剂盒包含所有必需的试剂,可立即用于PCR测试。 试剂和样品制备,预处理(加热),反应和检测的整个过程可以在大约一小时内完成。 无需复杂的RNA提取工作,只需将样品与处理溶液混合并加热即可,从而减少了人力并防止了人为错误。 即使使用96样品PCR装置测试了96个样品,也可以在不到一个半小时的时间内执行(混合处理液需要15分钟,热处理需要5分钟,PCR需要65分钟,总共85分钟)。
2。 提高准确性
向该试剂盒的反应混合物中添加参考组分,以确认扩增过程已正确进行,因此尽管由于操作不当等导致阳性结果,也不会发生基因扩增。我是这样可以减少假阴性的可能性,并提高测试结果的准确性 注意:该试剂盒是研究试剂。根据《药品和医疗设备法》,尚未将其批准为体外诊断药物或将其认证为体外诊断药物。但是,使用美国国立传染病研究所指定的评估方法以及保险涵盖的“ 2019-nCoV基因检测方法以及使用临床标本进行评估的结果”来验证性能(2020年4月9日)日语版)。评估中的正匹配率和负匹配率均为100%。 使用该试剂盒需要PCR设备,移液器,恒温器,小型离心机和其他设备,以及样品和基因处理技术。不打算出售。
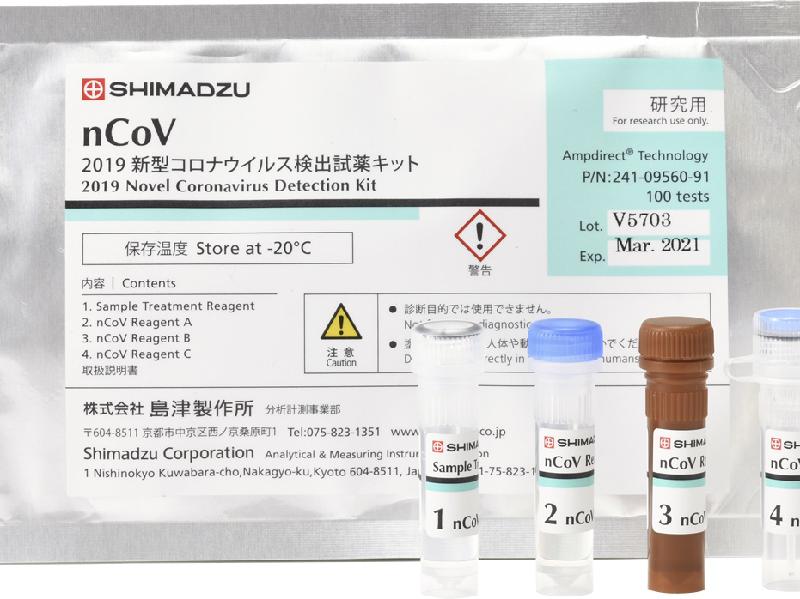
产品名称 “ 2019年新型冠状病毒检测试剂盒” 价格 225,000日元(100个样品/套,不含税) 月产量 100,000个样本
岛津制作所主页
https://www.shimadzu.co.jp/news/press/zfdyn69049lnnr8r.html
コメント
タグ